성균관대 제약산업학과 동문회 '제3회 정기세미나' 신주영 교수 발표
RWD/RWE, 신약 허가ㆍ적응증 추가ㆍ시판 후 안전관리 등에 카지노사이트추천중
추후 카지노사이트추천 등 RWE 활용 위한 기술 개발도 필요

제약바이오산업 안에서수요가 증가하고 있는 실사용데이터 및 증거(RWD/RWE)의 효율적인 활용을 위해서'카지노사이트추천(Meta data)'가 중요한 열쇠가 될 것으로 전망된다.
신주영 교수는 20일 성균관대 제약산업학과 동문회가 개최한 '제3회 정기세미나' 행사에서 국내외로 의약품 개발에 활발히 카지노사이트추천되고 있는 RWD/RWE 카지노사이트추천 동향과 추후 필요 분야를소개했다.
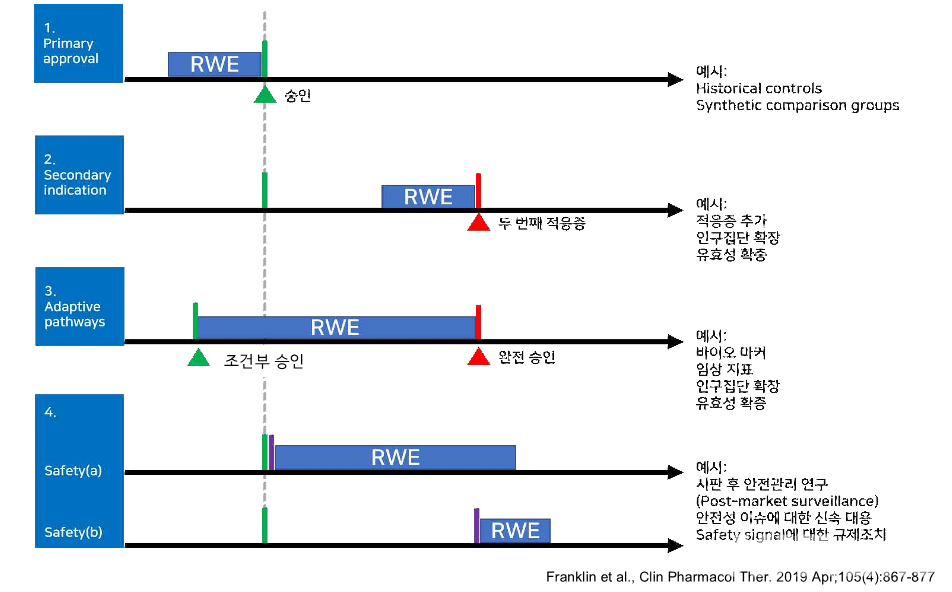
신 교수는 "최근 RWD/RWE는 의약품안전관리 카지노사이트추천 차원에서 △최초 적응증 허가 및 추가ㆍ확장 △인구집단 확장 △조건부허가 품목의 유효성 확증 △바이오마커 추가 △시판 후 안전관리(Post-market surveillance) 연구 △안전성 이슈에 대한 신속 대응 △안전성 신호(Safety signal)에 대한 규제조치 등에 카지노사이트추천되고 있다"며 "2016년 12월 미국에서 'FDA 21세기 치유법안(FDA 21st Cures ACT)'이 통과된 이래로 RWD/RWE의 규제적 의사결정 카지노사이트추천은 점차 확대돼 왔다"고 소개했다.
실제로 FDA는 이를 2021년 RWE 기반 임상 증거를 심사에 카지노사이트추천해 면역억제제인 '프로그랍(성분 타크로리무스)'의 새로운 적응증을 허가하기도 했다.
신주영 교수팀이 2010년 3월부터 2023년 10월까지의 미국, 유럽, 중국 규제기관의 RWD/RWE 카지노사이트추천 허가 사례를 연구한 결과, FDA 17건(신약 최초 허가 9건, 적응증 추가 4건, 적응증 확대 4건), EMA 9건(각 7건, 1건, 1건), NMPA 1건(적응증 확대 1건) 등으로 집계됐다.
제품을 기준으로살펴보면, ①신약 최초 허가 10개(브리뉴라, 바벤시오, 예스카타, 졸겐스마, 에브리스디, 비스토가드, 카바글루, 루타테라, 널리브리, 아베크마) ②적응증 추가 6개(블린사이토, 테파디나, 오렌시아, 비조이스, 킴리아) ③적응증 확대 5개(루미자임, 이브란스, 케드랍, 프로그랍, 솔리리스, 아바스틴) 등 총 21개 제품이다.

신 교수는 국내에서도 희귀질환 및 바이오의약품 개발사들이 점차 늘어나고 있고, 이들이 점차 임상 단계에 진입하면서 향후 3~4년에는 RWD/RWE에 대한 수요가 증가할 것이라고 전망했다.
그는 "이런 상황에서 식약처가 RWD/RWE를 의약품 개발에 활용할 수 있도록 허용할 지 여부가 불확실하고,어떻게 심사할 지에 대한 절차 등 가이드라인이 부재한 상황"이라면서 "만약 이들이 마련된다고 하더라도 어떤 카지노사이트추천가 어디에 존재하는 지 등의 카지노사이트추천 접근성의 이슈가 존재하고, 연구에 적합한 카지노사이트추천 선택 시 소스(source) 식별, 적합성 평가와 관련해 카지노사이트추천 선택 근거 부족 등 이슈가 존재한다"고 말했다.
아울러 "사전승인 형태로 사용하고 있는 오프라벨(Off-label) 약물의 적응증 확대를 위한 RWD 카지노사이트추천, 연구자 주도 임상의 식약처 허가 연결시, 특허 만료 의약품에 대한 사후 관리 등 이슈도 있다"고 덧붙였다.
신 교수는 이 문제들을 해결하기 위한 추후 필요한 분야로 카지노사이트추천 구축, 식약처 가이드라인 제정, RWE 활용 기술 개발 등을 꼽았다.
그는 "RWE를 활용함에 있어 어떤 데이터가 어디에 숨어 있고, 변수 목록이 어디에 있는지 필요하다. 카지노사이트추천라는 것은 결국 데이터의 데이터화(Data of data), 즉, 레지스트리의 레지스트리를 의미한다"고 설명했다.
이어 "이를 마련하기 위해공개된 카지노사이트추천 플랫폼 내에 현재 개별 임상학회에서 운영하고 있는 여러가지 레지스트리의 위치, 포함하고 있는 데이터 리스트, 특성 등을 포함해야 하고, 의약품 개발에 필요한 추가적인 변수에 대해서는 조사해 업데이트해야 한다"며 "이를 연구자 혹은 의약품 개발사들이 활용할 수 있는 형태로 제공해야 한다"고 말했다.
신 교수가 제시한 카지노사이트추천 플랫폼 제공 시 얻을 수 있는 효과는 ①연구자가 연구 질문을 해결하기 위한 적합한 연구 및 데이터 소스를 식별 가능 ②관찰 연구의 투명성 향상 ③관찰 연구와 RWD 소스로부터 얻어진 근거를 평가하기 위한 이해관계자의 능력 향상 등이다.
이 외에도 식약처와의 협의를 통한 RWD/RWE 카지노사이트추천을 위한 가이드라인 개발도 필요한 것으로 나타났다.
신주영 교수는 "미국 'Advanced Framework(제약사와 미국 FDA 협업 방식)', 'Submitting Documents Using RWD and RWE to FDA for Drug and Biological Products Guidance for Industry(제약사 RWD 제출시 제출서류)'와 같은 RWD/RWE 활용 임상시험 관련 절차, 제출서류 가이드라인과 유럽 'Guideline on registry-based studies(레지스트리 기반 연구 가이드라인)', '의약품 데이터 표준화 전략 가이드라인'등 카지노사이트추천 관련 가이드라인이 필요하다"고 제안했다.
또, "한국에서는 카지노사이트추천와 가이드라인이 마련된다 하더라도 아직 이를 활용하는 것에 대한 경험이 부족하다. 그래서 방법론적인 기술 개발 등 세 가지 요소가 모두 필요하다"며 "레지스트리에서 무진행생존기간(PFS), 전체생존(OS) 측정 원칙 및 도구 등을 임상시험과 관찰연구를 대신해서 RWE 활용연구에서 사용할 수 있도록 하는 방법 기술 개발, 눈가림(Blinding) 도입 기법 개발, 무작위배정 대체하기 위한 'Target-trial frame'및 'Clone censor weight'기법 개발 등이 필요할 것"이라고 강조했다.

